中国粉体网讯
最新JACS:揭开锂和钠在干燥空气中的反应之谜!
随着人们对电子设备的需求日益增加,石墨等经典电极将无法满足电池能量密度方面的高要求。锂金属是在阳极侧实现高能量密度的解决方案之一(图1a)。虽然锂金属在潮湿的空气中高度不稳定,而其在干燥的环境中具有相对较高的空气稳定性,这使得大规模制造锂金属电池成为了可能。与此同时,金属钠也是一种具有高能量密度的阳极,可用于电网存储的钠基电池;然而,即使是在干燥的空气中,钠也是不稳定的,这一特性阻碍了其进一步的应用。就动力学而言,在干燥的空气中,Li是稳定的,而Na是不稳定的,这一现象尚未被人们完全理解。在生产和运输过程中,Li或Na与环境气体之间的接触初步构成了固体电解质界面(SEI),从而为电池系统中随后的电化学和化学腐蚀反应设定了初始条件。因此,迫切需要从碱金属阳极电池的安全性和稳定性的角度来阐明碱金属在干燥空气中的界面钝化化学。
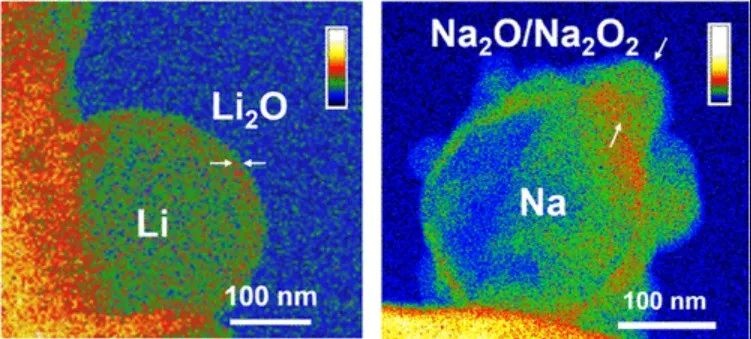
鉴于此,中国科学院物理研究所胡勇胜研究员、陆雅翔副研究员、肖睿娟副研究员联合燕山大学黄建宇教授将原位环境透射电子显微镜与理论模拟相结合,揭示了Li和Na在干燥空气中的稳定性迥异的原因。该解释认为,Li金属上形成致密的Li2O层,以及Na金属上形成多孔和粗糙的Na2O/Na2O2层是在2环境中不同热力学和动力学的结果。作者还提出了一种防腐策略:预先在Na的表面形成碳酸盐层可以改变其动力学,使其具有防腐性能。该研究加深了对与环境气体相关的化学反应的理解,并通过控制界面稳定性提高了Li和Na的电化学性能。该工作以题为“Unraveling the Reaction Mystery of Li and Na with Dry Air”的论文发表在最新一期《Journal of the American chemical society》上。

Li/Na在干燥空气中反应的微米级表征
在干燥的环境(~0%RH)中,新鲜Li和Na会发生宏观上的变化(图1c)。在干燥空气暴露20分钟后, Li几乎没有颜色变化,但Na的表面失去了光泽(产物分别表示为A-Li和A-Na)。冶金显微镜的非原位观察表明,A-Li的金属条纹仍然存在(图1d,e),而在干燥的空气中,A-Na有一个暗覆盖层(图1f,g)。扫描电子显微镜(SEM)图像显示,A-Li的表面光滑,有几个微小的腐蚀点,如图1h–j所示。而在A-Na中可观察到多个宽度为1–2μm的随机分布裂纹(图1k–m)。显然,空气可以持续渗透到裂纹中,并与内部新鲜的Na发生反应。原子力显微镜(AFM)检测到, A-Na的表面比A-Li的表面粗糙度更大。微观上,表面积相对较大的A-Na钝化层与A-Li钝化层相比能接触到更多的空气。
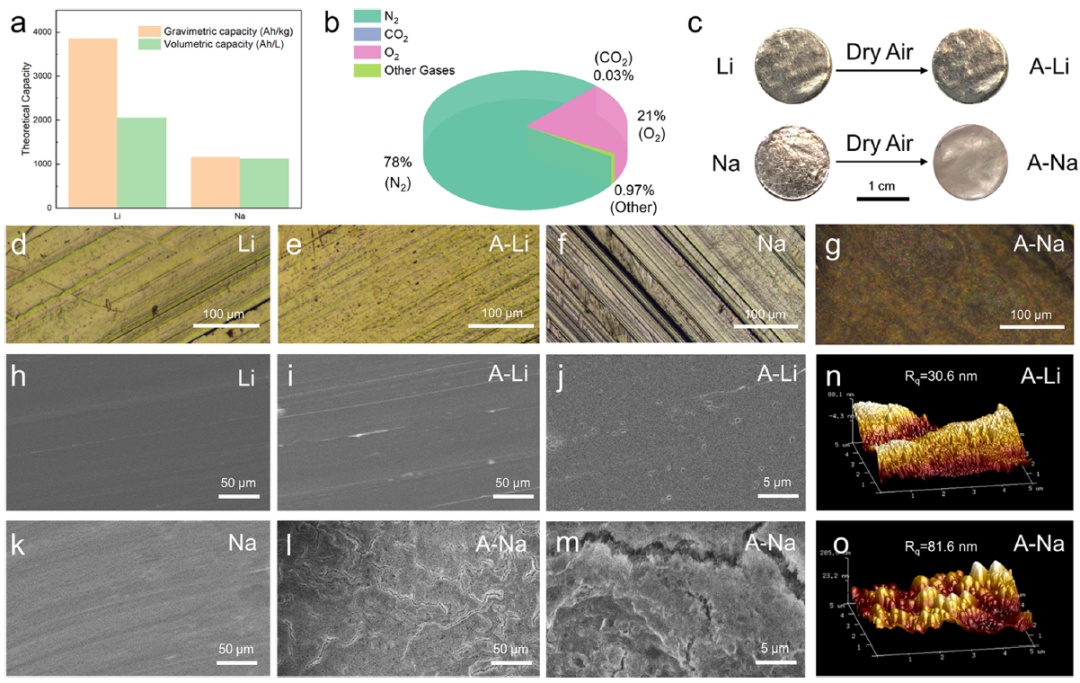
图1. 干燥空气中Li和Na表面层的微米级研究。
作者通过原位环境透射电子显微镜(ETEM)观察,发现当1毫巴的干燥空气流入ETEM室时,Li的形态几乎没有变化,但在大约3小时后,Na的内部出现了空隙。内部Na的快速损失可归因于Kirkendall效应,该效应是由于Na+的迁移速度比O2-的迁移速度快,导致向内和向外质量扩散之间的巨大差异。干燥的空气显著增厚了Na的钝化层,表现出粗糙和松散的形态(图2g,h)。然而,Li的钝化层厚度仅略有增加,呈现为薄而平坦的表面(图2b)。
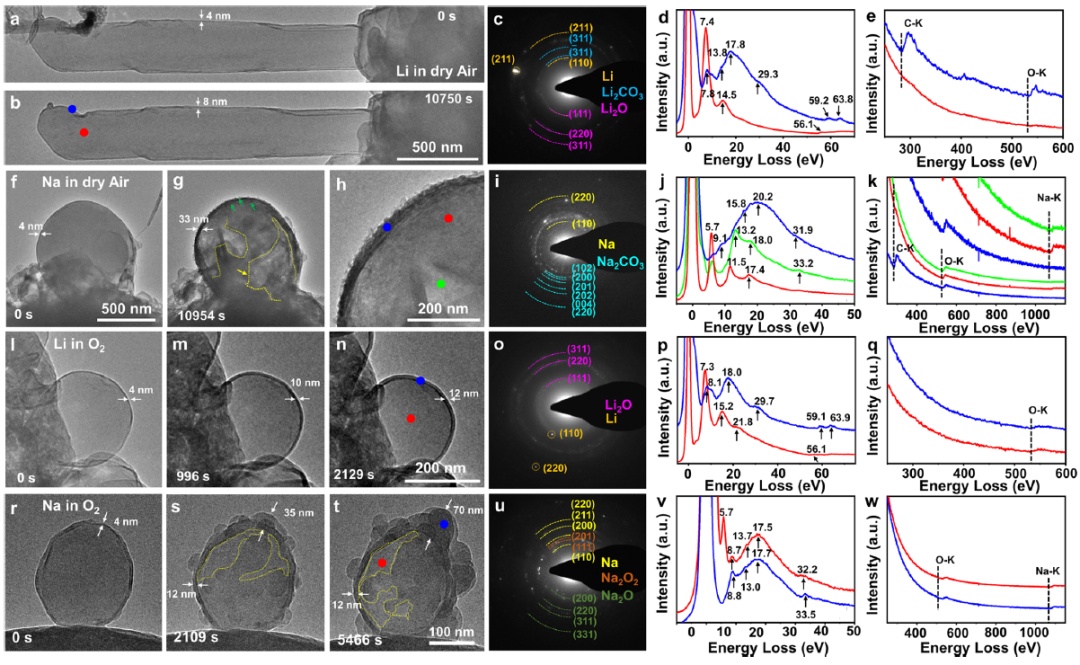
图2. 在干燥空气或O2中Li和Na表面层形成过程的纳米级原位ETEM研究。
Li/Na在干燥空气中反应的热力学和动力学计算
作者通过吉布斯自由能的计算,发现在热力学的角度,由Na2O形成Na2O2比由Li2O形成Li2O2更有利。为了解释整个现象,作者通过密度泛函理论(DFT)计算研究了O2在M(Li或Na)和M2O上的初始吸附机制。能量最低的最稳定配置如图3a–d所示。计算表明,O2会在Na2O上快速吸附,而在Na上进行相对缓慢的吸附。O2在Na表面上的吸附经历了一个非离解过程,这表明其吸附能略高于在Na2O上的吸附能。因此,当O2攻击时,Li是Li/Li2O界面中的优先吸附基质,但根据计算,这种优先级在Na系统中不太清楚(O2对Na2O甚至可能在动力学上更有利)。接着,作者通过进一步的动力学计算,提出了Li和Na与氧的特定反应机制(图3i,j)。在Li–O2体系中,O2在缺陷等活性位点上发生初始吸附后,立即形成Li2O。随后的O2吸附仍然优先发生在新鲜的Li位点,而不是在Li2O上,导致Li2O的产物呈现为完整且紧凑的覆盖堆叠,该过程一直持续到不再存在新鲜的Li。该体系中的低扩散速率防止了通过传质形成厚的Li2O,并且单一产物(Li2O)也诱导了均匀的Li扩散通量。而在Na–O2系统的情况下,O2在Na和Na2O上的吸附具有相似的概率,导致不同Na2O岛之间的初始尺寸分布相对较大。小的Na2O岛倾向于扩散并合并成大岛,以减少表面能。同时,基于Na2O的Na2O2的形成可以进一步增厚钝化层,并且通过Na2O/Na2O2存在不利的界面扩散,导致Na2O/Na2O2生长不均匀(不足的Na离子倾向于优先聚集在尖端,这类似于金属的枝晶生长机制)。在进一步暴露于CO2时,Li系统在先前均匀且薄的Li2O的基础上产生均匀的Li2CO3,这使得大块Li在干燥空气中稳定且有光泽。相反,Na上的钝化层是粗糙和多孔的,因为首先形成Na2O/Na2O2层,然后形成Na2CO3,其中Na2O2和CO2反应产生的新O2可能逸出,导致许多空隙和孔,这些空隙和孔可能由于Kirkendall效应而破裂。因此,具有许多裂纹的多孔钝化层会导致干燥空气中Na的快速失效。尽管Li+的移动速度也比O2-快,但在Li系统中没有Kirkendall扩散,因为Li2O的薄而紧凑的覆盖层可以保护Li金属不与氧气发生过多反应。
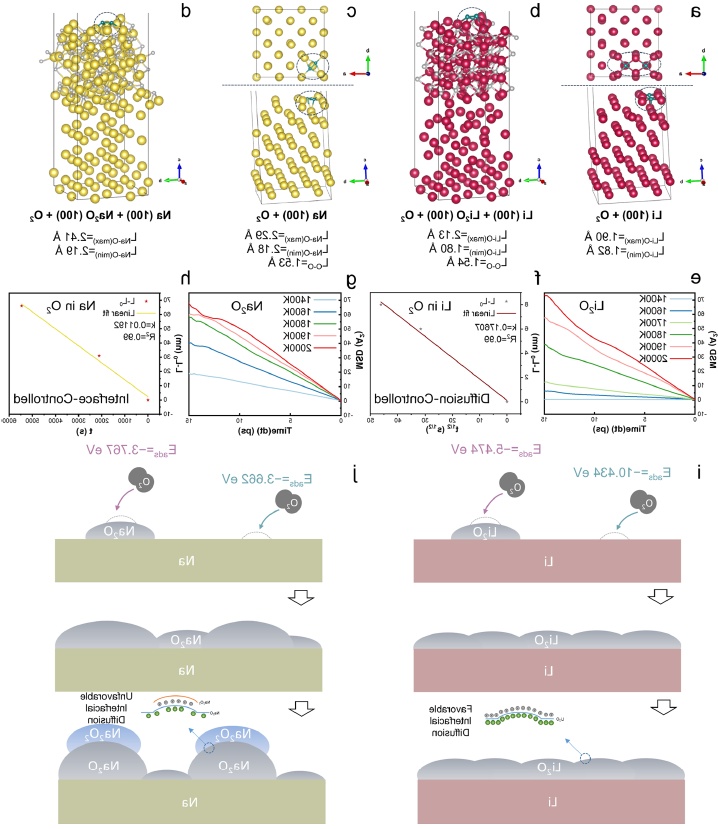
图3. O2中Li和Na的热力学和动力学计算。
预设碳酸盐钝化层来实现Na的防腐为了使Na在干燥空气中保持稳定,可在氧化过程之前引入保护层。为此,作者采用CO2处理以产生均匀的Na2CO3层。当CO2与新鲜Na接触时,逐渐形成结晶度均匀且厚度很薄的钝化层(图4a–d)。随后,将气体环境从二氧化碳转换为干燥空气。研究发现,干燥的空气不能破坏Na2CO3覆盖的Na颗粒,在没有其他成分的情况下,膜厚度缓慢稳定地增长到10 nm(图4e–h,j)。此外,在第二步中用O2代替干燥空气时,紧凑型Na2CO3甚至可以保护Na免受O2的侵蚀。为了解释这一现象,作者通过BV方法证实Na+在Na2CO3中的迁移势垒高于O2-(图4k),这导致Na+的缓慢扩散,并限制了Na2CO3的进一步生长。
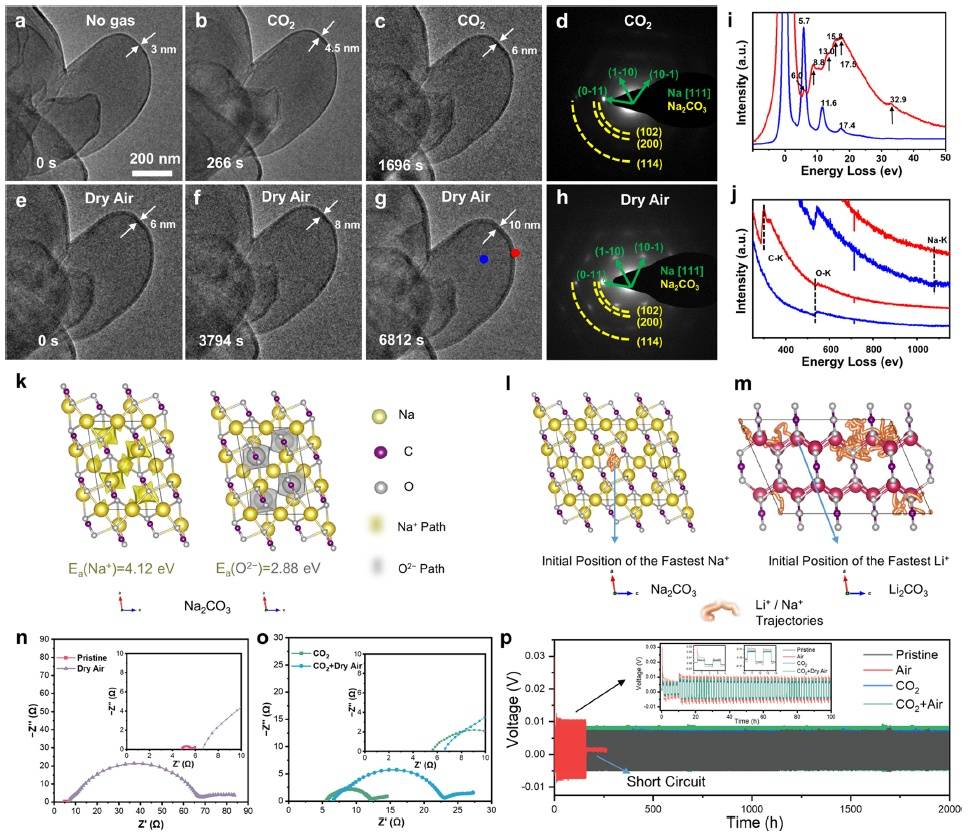
图4. 预设碳酸盐钝化层。
小结
该工作在实验表征和理论模拟的基础上,对Li/Na与干燥空气之间腐蚀反应的详细物理化学过程提出了全新的见解。与之前对Li和Na之间相对于氧的不同化学活性的解释截然不同,该工作提供了一幅微观图像。Li基和Na基反应之间的热力学和动力学差异导致微观和宏观形态的变化,这严重影响了它们在空气中的稳定性。作者还提出了一种提高Na表面稳定性的策略:形成适当的人工SEI(例如,通过暴露于CO2形成的Na2CO3),解决了自发形成质量较差的氧化物基钝化层的问题。无定形人工SEI膜的生长可能实现更致密的SEI。这种方法也可以推广到其他受腐蚀影响的储能设备上。对于M2O、M2O2和M2CO3的详细分析(结晶度、形态特征、扩散特性等)也有助于理解实际电池系统中SEI的孔隙率和生长,从而实现Li和Na的可控界面化学。
(中国粉体网编辑整理/乔木)
注:图片非商业用途,存在侵权告知删除!

















