中国粉体网讯 散剂系指原料药物或与适宜的辅料经粉碎、均匀混合制成的干燥粉末状制剂。
散剂可分为口服散剂和局部用散剂。
口服散剂一般溶于或分散于水、稀释液或者其他液体中服用,也可直接用水送服。
局部用散剂可供皮肤、口腔、咽喉、腔道等处应用;专供治疗、预防和润滑皮肤的散剂也可称为撒布剂或撒粉。
散剂在生产与贮藏期间应符合下列有关规定。
一、供制散剂的原料药物均应粉碎。除另有规定外,口服用散剂为细粉,儿科用和局部用散剂应为最细粉。
二、散剂中可含或不含辅料。口服散剂需要时亦可加矫味剂、芳香剂、着色剂等。
三、为防止胃酸对生物制品散剂中活性成分的破坏,散剂稀释剂中可调配中和胃酸的成分。
四、散剂应干燥、疏松、混合均匀、色泽一致。制备含有毒性药、贵重药或药物剂量小的散剂时,应采用配研法混匀并过筛。
五、散剂可单剂量包(分)装,多剂量包装者应附分剂量的用具。含有毒性药的口服散剂应单剂量包装。
六、除另有规定外,散剂应密闭贮存,含挥发性原料药物或易吸潮原料药物的散剂应密封贮存。生物制品应采用防潮材料包装。
七、散剂用于烧伤治疗如为非无菌制剂的,应在标签上标明“非无菌制剂”;产品说明书中应注明“本品为非无菌制剂”,同时在适应证下应明确“用于程度较轻的烧伤(Ⅰ°或浅Ⅱ°)”;注意事项下规定“应遵医嘱使用”。
除另有规定外,散剂应进行以下相应检查。
【粒度】除另有规定外,化学药局部用散剂和用于烧伤或严重创伤的中药局部用散剂及儿科用散剂,照下述方法检查,应符合规定。
检查法 除另有规定外,取供试品10g,精密称定,照粒度和粒度分布测定法(通则0982单筛分法)测定。化学药散剂通过七号筛(中药通过六号筛)的粉末重量,不得少于95%。
【外观均匀度】取供试品适量,置光滑纸上,平铺约5cm2,将其表面压平,在明亮处观察,应色泽均匀,无花纹与色斑。
【水分】中药散剂照水分测定法(通则0832)测定,除另有规定外,不得过9.0%。
【干燥失重】化学药和生物制品散剂,除另有规定外,取供试品,照干燥失重测定法(通则0831)测定,在105℃干燥至恒重,减失重量不得过2.0%。
【装量差异】单剂量包装的散剂,照下述方法检查,应符合规定。
检查法 除另有规定外,取供试品10袋(瓶),分别精密称定每袋(瓶)内容物的重量,求出内容物的装量与平均装量。每袋(瓶)装量与平均装量相比较[凡有标示装量的散剂,每袋(瓶)装量应与标示装量相比较],按表中的规定,超出装量差异限度的散剂不得多于2袋(瓶),并不得有1袋(瓶)超出装量差异限度的1倍。
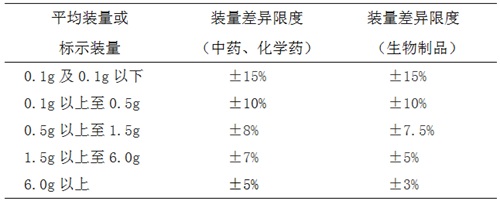
凡规定检查含量均匀度的化学药和生物制品散剂,一般不再进行装量差异的检查。
【装量】除另有规定外,多剂量包装的散剂,照最低装量检查法(通则0942)检查,应符合规定。
【无菌】除另有规定外,用于烧伤[除程度较轻的烧伤(Ⅰ°或浅Ⅱ°外)]、严重创伤或临床必需无菌的局部用散剂,照无菌检查法(通则1101)检查,应符合规定。
【微生物限度】除另有规定外,照非无菌产品微生物限度检查:微生物计数法(通则1105)和控制菌检查法(通则1106)及非无菌药品微生物限度标准(通则1107)检查,应符合规定。凡规定进行杂菌检查的生物制品散剂,可不进行微生物限度检查。
(中国粉体网编辑整理/青黎)
注:图片非商业用途,存在侵权告知删除