中国粉体网讯 近年来,在医学上主要用于矮小症的“增高针”治疗正在悄然兴起,引发市场关注。另一方面,很多家长对于孩子的身高太焦虑,想通过使用生长激素来改善身高,国内生长激素市场发展迅速。
生长激素即由人体脑垂体前叶分泌的一种肽类激素,它由191个氨基酸组成,能促进骨骼、内脏和全身生长,并促进蛋白质合成,影响脂肪和矿物质代谢,在人体生长发育中起着关键性作用。
目前已上市的生长激素主要有三大类别,分别是:每天注射一次的重组人生长激素注射用冻干粉针剂(即短效粉针)和重组人生长激素注射液(短效水针),以及每周注射一次的聚乙二醇重组人生长激素注射液(长效水针)。
随着技术迭代,目前生长激素市场的竞争,已聚焦在长效剂型。该剂型注射频率为一周一次,大大提高了患者对生长激素疗法的接受度、耐受性等。
长效生长激素全球市场
现在全球有4款长效生长激素获批上市,分别是长春高新子公司金赛药业的金赛增、诺和诺德的Sogroya、Ascendis的Skytrofa和辉瑞的Ngenla。
其中金赛增是全球第一支聚乙二醇(PEG)化长效生长激素制剂,也是我国唯一上市的长效生长激素制剂,金赛药业也因此成为国内唯一拥有完整的粉针剂、水针剂、长效水针剂全产品线的生长激素厂商。
诺和诺德的Sogroya于2020年9月获FDA批准上市,用于治疗成人生长激素缺乏症(AGHD),是FDA批准的首款成人长效人生长激素。2023年4月,Sogroya获FDA批准扩大适应症,用于治疗2.5岁及以上儿童的生长激素缺乏症。
丹麦药企Ascendis的Skytrofa于2021年8月获FDA批准,用于治疗1岁及以上儿童的生长激素缺乏症。
辉瑞的Ngenla于2023年6月获FDA批准,用于治疗3岁以上内源性生长激素分泌不足导致生长缓慢的儿童患者。
国内生长激素市场
在国内,根据中华医学会的数据,因生长激素缺乏症而真正接受治疗的患儿不足3万名,药物治疗渗透率不到1%。相比于欧美发达国家10%以上的渗透率,国内生长激素市场存在巨大的提高空间。
看好国内市场,目前,诺和诺德的Sogroya和Ascendis的Skytrofa已在国内进入III期临床试验阶段。其中Ascendis的Skytrofa(隆培促生长素)的大中华区权益由国内维昇药业获得,隆培促生长素是一种新型的未经修饰的长效生长激素剂型,其制备过程为将生长激素暂时连接到长效载体形成前药,在一定时间内在体内释放。
十年来,金赛药业在国内长效生长激素领域一直一家独大。聚乙二醇重组人生长激素注射液金赛增是一种注射频率为每周1次的长效生长激素,于2014年1月在中国获批上市,规格为54IU/9.0mg/1.0ml/瓶,适应症为内源性生长激素缺乏所引起的儿童生长缓慢。目前,其适应症已达12种,且还有新适应症处于审批阶段。
根据米内网数据,近年来在中国公立医疗机终端,聚乙二醇重组人生长激素销售收入逐年攀升,由2020年约4亿元增长至2022年超7亿元;2023上半年突破5亿元,同比增长46.37%。
生长激素市场吸引了国内多家企业入局。
1月10晚间,特宝生物公告称,公司怡培生长激素注射液上市申请获国家药监局受理。特宝生物公告显示,怡培生长激素注射液采用40kDY型分支聚乙二醇(YPEG)分子对人生长激素(rhGH)进行单分子修饰,优选高生物学活性、非N-末端位点为主的修饰组分,在保证疗效的同时,旨在降低给药剂量,获得更佳的长期药物安全性。
天境生物/济川药业的伊坦长效生长激素(TJ101)则通过Fc片段融合蛋白的方式,延长了半衰期,具有半个月注射1次的可能;同时,其分子改造没有引入外源物质,最大程度上避免了肾毒性等问题。目前,TJ101 III期临床已经成功,潜在价值释放在即。在商业化方面,TJ101由儿科领域拥有显著渠道优势的济川药业负责。天境生物计划在2024年提交伊坦生长激素的上市申请。
安科生物自主研发的长效生长激素产品“AK2017注射液”也曾于2022年10月获得了国家证监局临床试验批件。
随着竞品增多,原本未被充分开发的生长激素市场也将变得拥挤。
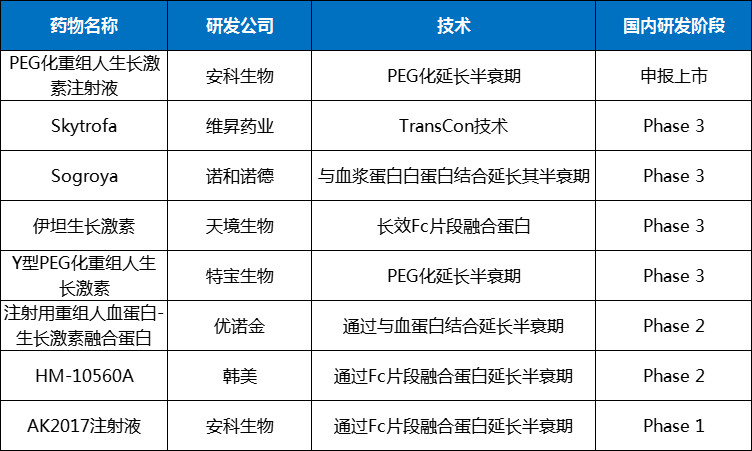
(来源:药智网整理)
3月1日,《生长激素制剂用于生长激素缺乏症临床试验技术指导原则》施行
为规范和指导生长激素缺乏症新药的研发,在国家药品监督管理局的部署下,药审中心组织制定了《生长激素制剂用于生长激素缺乏症临床试验技术指导原则》,自3月01日发布之日起施行。
重点内容:
1、为尽量减少其他因素对研究结果评价的干扰,建议首先在健康成人受试者中开展单次给药剂量递增研究,以考察试验药物初步的耐受性、安全性、药代动力学(Pharmacokinetics,PK)及免疫原性特征。
2、在充分评估受试者单次使用生长激素制剂的安全性风险后,Ⅰ期临床试验多次给药剂量递增研究也可在儿童原发性GHD患者和成人GHD患者中进行。
3、IGF-1是生长激素活性的药效动力学标志物,此外,也可以使用胰岛素样生长因子结合蛋白3进行PD评价。由于 IGF-1 水平和疗效之间缺乏明确的对应关系,IGF-1 不能作为生长激素确证性临床试验疗效的替代指标。
4、儿童原发性GHD一般情况下推荐基于体重的给药方案。成人GHD推荐从低剂量起始的滴定给药方案,在既往同类产品临床研究中,观察到接受剂量滴定的成人GHD受试者不良反应的发生率更低。
5、综合早期健康受试者及患者研究的安全性、耐受性、PK、PD及初步有效性数据,在合理剂量范围内选择Ⅱ期探索性研究的推荐剂量。通常,试验组建议不少于3种给药方案,研究治疗观察周期不少于 24 周。
生长激素国外市场也蕴藏发展潜力,未来长期成长可期
据Frost&Sullivan数据,2018-2030年,全球儿童生长激素缺乏症的治疗市场规模均按照年复合增长率6.4%递增,到2030年将达60亿美元。目前海外市场国内龙头企业也在积极布局,长春高新长效生长激素有望直接进入美国III期临床,并努力争取在2027年上市,安科生物也在加速布局海外业务。
参考来源:
金融界:“东北药茅”要被抢饭碗?特宝生物生长激素新药上市申请获受理,长春高新曾靠此赚了数十亿元
药渡Daily:长效生长激素迎来新入局者,百亿市场格局生变
药春秋:“一品独大”的长效生长激素,谁将拿下第二家?
国家药监局药审中心:2指导原则发布→小儿便秘中药新药、生长激素制剂
药智网:谁将成为下一个“生长激素王者”?
民生证券:医药行业专题报告:长效剂型生长激素快速放量,产品出海未来可期
(中国粉体网编辑整理/青黎)
注:图片非商业用途,存在侵权告知删除