中国粉体网讯 目前,生物制药行业发展迅速,尤其是上游表达量的增加和规模的扩大,常规的批次生产效率有限,而连续流生产在提高产能、降低成本和缩短时间上显示出广阔的应用前景。
背景介绍
中国的生物制药行业才刚起步,中国药企无论在技术水平还是生产规模及效率上都与国外生物药巨头有较大差距,如果还是按国外原研药的批次生产模式,生产成本就没有优势,在带量采购的竞标中就会处于劣势。因此中国生物药企业要在激烈竞争中获胜,就必须比原研药厂拥有更好的生产工艺、更高的生产效率及更低的生产成本。应用连续生产工艺技术将是中国生物药获得竞争优势的一个突破口。连续生产技术刚刚起步,国内外基本处于同一起跑线上,如果中国生物类似药企业可以抓住机遇优先发展和使用连续生产工艺,将可以发挥后发先至的优势,提高生产效率,降低生产成本。
传统生物药生产采用的是批次生产流程,需要经历一系列间隔的生产步骤。整个流程中的每个间隔环节都会带来生产效率的降低和延迟,并增加产品缺陷和操作失误的概率。连续生产制药技术是一种新兴技术,虽然还面临着许多监管的问题和技术的挑战,但连续生产的优越性却显而易见,也是生物制药工艺发展的大势所趋,能够提高生产过程的稳健性和可靠性、降低生产和固定资产支出、减少工厂建造时间、降低生产中产品更换所需时间。
在下游生产过程中,连续流的实现主要通过采用连续流层析、在线检测等技术将多个工艺单元进行整合(Figure 1),可以在提高生产效率与厂房利用率的同时,减小中间体存储量、各步骤之间的等待时间以及仪器设备所需的规模和对应的投入,从而达到缩短生产周期与降低生产成本的目标。

Figure 1 整个下游的工艺控制流程图
Note:利用实时的检测手段来控制工艺过程
案例分析
就下游的分离纯化过程而言,主要包括:包括第一步用Protein A 亲和介质捕获抗体; 第二步用阳离子层析作为中间纯化去除抗体多聚体、HCP、DNA等,第三步用阴离子层析介质精细分离残留的DNA,、HCP、Protein A、内毒素等杂质以达到精纯目的(Figure 2)。

Figure 2下游纯化过程
下游纯化工艺的主要目的是通过分离纯化提高产品的纯度和收率,保障产品质量和稳定性。连续生产需要把所有步骤连接起来,使得生产工艺可以高度集成,高度自动化,而且要确保产品的稳定性和一致性等(Figure 3)。
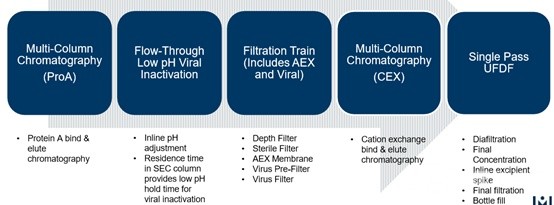
Figure 3连续流下游纯化总流程
连续流工艺可以提高填料的利用率,缩短工艺时间,提高产能(Figure 4)。下面将从几个案例介绍连续流工艺的应用。

Figure 4连续流工艺提高效率
案例一:连续捕获
DF的当前工业实践是手动操作模式,为了升级系统以进行连续收获,可以如下图5所示设计过滤器支架。每一轮过滤器可以顺序执行。每次完成DF后,都可以使用新的过滤器对固定器进行拆卸和重新组装。可以设计这种类型的硬件,并将其用于将来的连续DF。

Figure5连续捕获的深层过滤系统
案例二:Cytiva的PCC在亲和层析过程的使用
连续mAb捕获已成功地从工艺开发实验室应用于大型生物制药公司的生产规模,连续捕获可提高效率,保证产品质量(缩短HCCF的存储时间)。例如,Cytiva PCC连续流技术,采用多根层析柱,在纯化过程中,这几个柱子在上样、淋洗、洗脱、再生之间交替进行。这种方式可以充分利用填料的最高载量(Figure6),详细流程图见Figure 7。
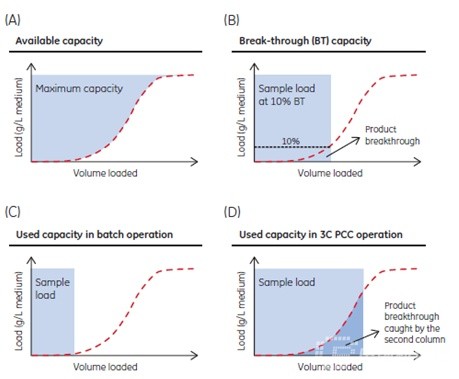
Figure 6 PCC模式下填料载量利用情况
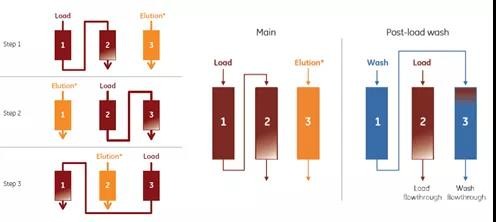
Figure 7 三柱PCC流程图
因此,PCC技术三个优势:
(1)减少填料的使用量降低填料成本(Table 1);
(2)减少buffer的消耗(3)缩短工艺时间
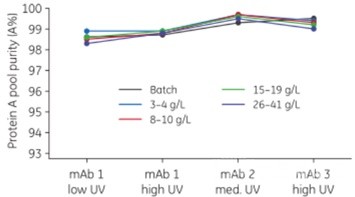
(3)不受制于上游的培养工艺(5)在下游纯化过程中,与传统批次生产相比,对产品质量的影响非常类似(Figure 8).
Table 1传统批次生产与连续流生产的填料消耗比较
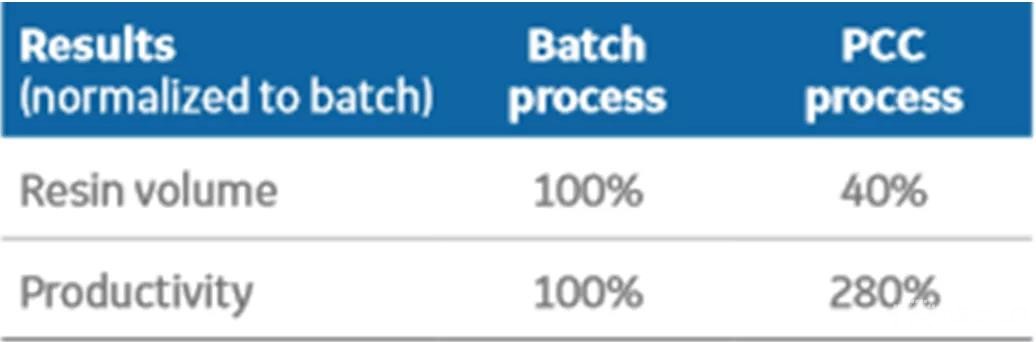
Figure 8 连续流工艺在高载下的表现
案例三连续流在pH病毒灭活中的应用
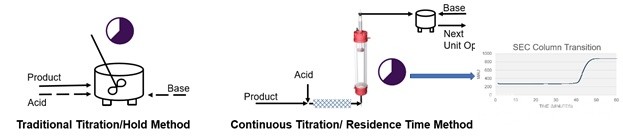
Figure 9 Continuous flow design for Viral Inactivation
在线稀释操作使低pH的病毒灭活的连续生产成为可能(Figure 9)。通过pH计监控实时的产品的pH情况,除此外应当仔细研究洗脱中批次之间的pH变化,以了解洗脱缓冲液pH和柱负载密度变化的影响。低pH保持后的单克隆抗体聚集应受到密切监控,SEC层析柱实时监控蛋白的质量,防止酸碱滴定过量造成变性聚集。如果mAb对低pH处理敏感,则可以选择去污剂处理(例如1%v/v聚山梨酯20+0.03%磷酸三正丁酯),因为它可以在五分钟内有效灭活包膜病毒(例如>5对数减少)
案例四 Cytiva的PCC在蛋白精纯过程的使用
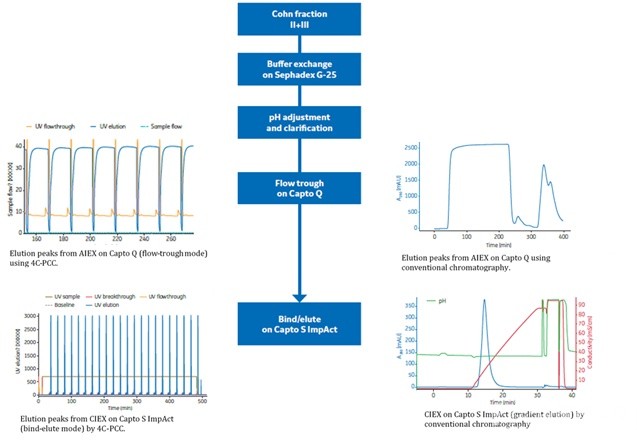
Figure 10 连续流在IgG纯化中的应用
将连续流工艺用在IgG Cohn fraction II and III纯化工艺中(Figure 10),与传统的批次工艺相比,PCC技术用在AEX流穿模式和CEX结合洗脱模式下,其工艺表现经过多个cycle后依然保持一致,产品质量经分析检测也能达到预期标准(Figure 11 )
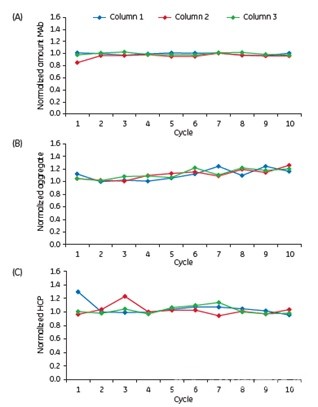
Figure 11 PCC技术中产品中的杂质残留
Note:(A) Amount MAb, (B) aggregate content, and (C) HCP contentin elution pool from the 3C-PCC setup.
案例五:Cytiva的PCC在疫苗生产过程的使用
今年新冠病毒的泛滥使疫苗的产业又迅速回归大众的视线,连续流工艺能够通过不间断的流程以更快、更稳定、更经济、更安全地生产,下图12为PCC技术在疫苗产业的应用。
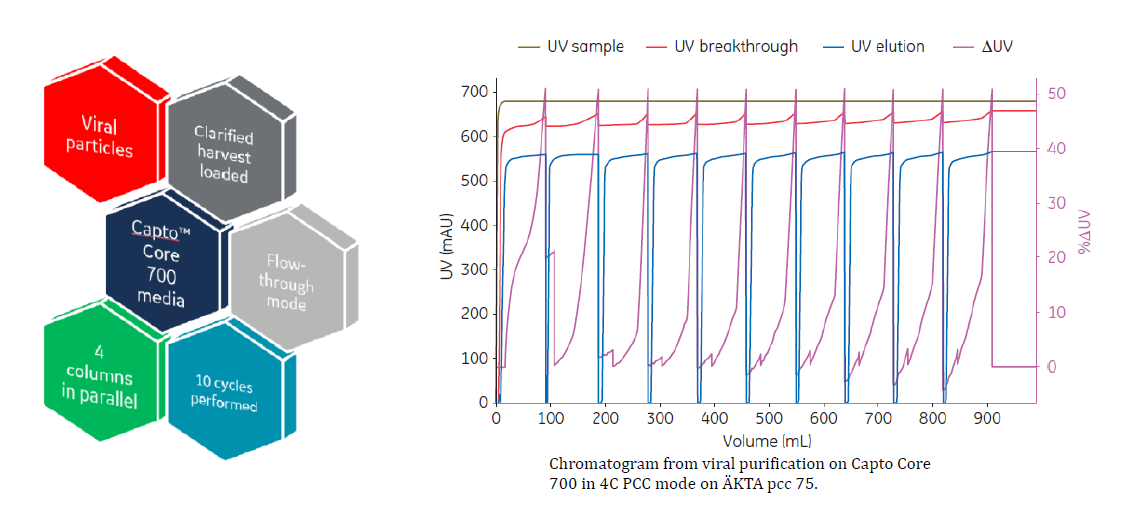
Figure 12 4C-PCC在疫苗产业中的应用
①ÄKTA PCC 75连续10 cycles都能够保持较好的工艺
②纯度和收率都能达到预期水平
③基线控制和动态UV控制有效的适用到连续流技术中
④图谱的趋势分析能够及时的监控工艺,实时质量监控,随时撇下不达标的中间产品,使其确保稳定持续的产品质量
⑤系统能够精准的操作结合洗脱的模式,对流穿模式有一定的局限性
⑥连续生产还可以提高介质利用度,降低流动相及介质的使用量从而降低生产成本
案例六:Cytiva的PCC放大过程
目前,PCC技术正在从实验室规模到生产规模的转变实验阶段(Figure 13),可以得到50倍放大到294倍放大(Table 2)。数据显示,放大后的生产工艺的可持续性和产品的质量都能达到预期的结果。

Figure 13 PCC技术从实验室规模放大到生产规模
Note:(A) Lab-scaleÄKTA pcc, with UNICORN™ control software,
(B) BioProcess pcc, with UNICORN software and DeltaV™ distribution controlsystem,
Table 2 从实验室规模到生产规模的放大
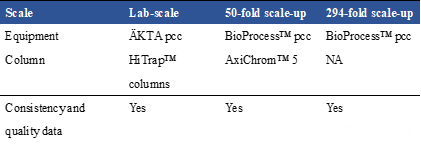
Table 3 传统生产批次与连续流生产(2000L)的质量数据比较
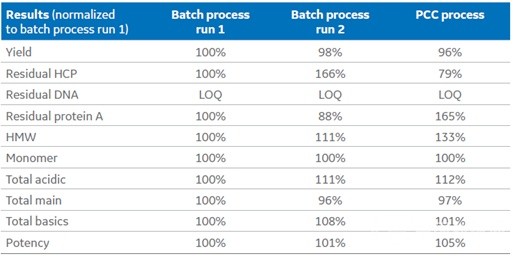
放大到2000L的规模,产品的质量和回收率能够很好的得到保证(Table 3),并且连续流工艺显示出较好的优势:
①填料使用量有65%的降低
②Buffer使用量有40%的降低
③人力成本有33%的降低
④连续流技术的应用更依赖于PAT技术的支持
FDA已将过程分析技术(PAT)定义为通过及时测量影响关键质量属性(CQA)的关键过程参数(CPP)来设计、分析和控制生产过程的系统。PAT包括大量的化学、物理和统计分析,以及各种分析测量,包括热电偶、红外、拉曼和紫外光谱、质谱、色谱、核磁共振、结晶监测以及粒子大小分析(图14)。在软件的帮助下,PAT可以与下游装置进行自动化合成,用反馈系统控制反应条件和优化代替筛选实验。

Figure 14 可用于连续流工艺的PAT的代表性范例
结束语
连续生产制药技术是一种新兴技术,需要解决上游连续细胞培养技术和下游分离纯化技术,其中最具挑战的是下游分离纯化。虽然还面临着许多监管的问题和技术的挑战,但连续生产的优越性却显而易见,也是生物制药工艺发展的必然趋势。
首先,由于连续生产工艺集成度高、自动化程度高,因此可减少人工成本。第二,连续生产还可以做到实时质量监控,从而让产品质量更可靠。第三,连续生产可以实现设备小型化,高效利用厂房空间,大幅度缩小厂房的使用面积,减少固定资产的投资。第四, 连续生产还可以提高介质利用度,降低流动相及介质的使用量从而降低生产成本;第五, 连续生产规模易于调节,可大可小,方便适应不断变化的市场需求,这种操作灵活性同时减轻一些审批后的监管任务,也使得工艺更容易放大,减少传统工艺放大所面临的诸多验证和重复的问题。
(中国粉体网编辑整理/昧光)
注:图片非商业用途,存在侵权告知删除!