中国粉体网讯 3月6日,国家药品监督管理局食品药品审核查验中心发布《吸入制剂现场检查指南》,意在为进一步指导吸入制剂现场检查工作,帮助检查员识别吸入制剂的风险控制点,提高现场检查质量。

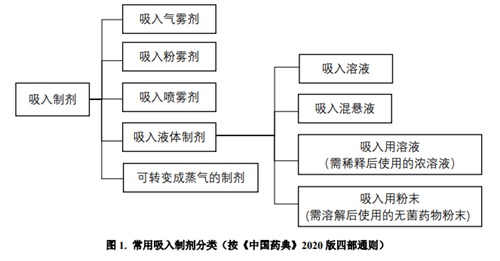
吸入制剂,系指原料药物溶解或分散于适宜介质中,以气溶胶或蒸气形式递送至肺部发挥局部或全身作用的液体或固体制剂。吸入后药物颗粒或雾滴在有效部位的沉积,对于吸入制剂的安全性和有效性至关重要。从支气管(第1级)至肺泡管共有21级,吸入药物的固体颗粒或液体雾滴只有在合适粒径范围内才能被递送至靶部位。通常来说,粒径小于5μm的颗粒或雾滴可有效到达肺部;如需进入外周气道,颗粒或雾滴粒径将更小。
《吸入制剂现场检查指南》重点内容
1、对采用“两步法”生产的品种需重点考察罐间递送剂量均一性。对于混悬型吸入气雾剂,还需额外关注原料药与辅料的粒径对微细粒子剂量的影响。
2、样品试制记录中,需关注各关键生产工艺的控制及关键工艺参数的确认和变化。如气雾剂生产工艺抛射剂添加、封阀、检重检漏、生产时限等过程控制,以及搅拌循环时间、存放时限、封阀参数和灌装量等关键工艺参数。
3、混悬型吸入气雾剂为保证足够剂量沉积于肺部,需控制原料药的粒径,一般应当在10μm以下,其中大多数应当在5μm以下,具体参数设置应当与申报资料一致。
4、需关注给药装置(如驱动器)对递送剂量均一性的影响,并进行原料药与辅料的相容性研究。
5、吸入气雾剂的稳定性研究重点考察项目需关注不同放置方位(正、倒、水平)有关物质、微细粒子剂量、递送剂量均一性和泄露率等。
6、处方工艺需关注与水分、递送剂量均一性、微细粒子剂量等与关键质量属性相关联的关键物料属性和关键工艺参数的筛选和确定。
7、吸入气雾剂包装通常包括罐体和阀门,需重点关注定量阀体积、罐体材质和驱动器孔径。
8、吸入气雾剂灌装全过程的药液含量均匀性需进行验证,应确保药液含量均匀性的过程控制方法和工艺参数。
参考来源:
国家药品监督管理局食品药品审核查验中心、《吸入制剂现场检查指南》、蒲公英ouryao等
(中国粉体网编辑整理/青黎)
注:图片非商业用途,存在侵权告知删除


















