中国粉体网讯
【研究背景】
固态锂金属电池由于其高安全性和高理论能量密度等优点而成为广受关注的新一代电化学储能设备。硫化物固体电解质具有和有机电解液(~10mS/cm)相当甚至更高的离子电导率而被广泛研究,但电解质与氧化物正极之间严重的界面副反应阻碍了硫化物电解质全固态电池长循环性能的实现。此外,全固态电池中正极匹配不同硫化物电解质的电化学性能差异非常明显,其内在机制尚不清楚,由于界面产物包埋在复合正极内部使得对其表征难度增大,难以对其进行准确定量,极大限制了对界面反应机制的研究。
【研究简介】
近日,厦门大学杨勇教授、龚正良教授团队通过热力学相平衡方法对复合正极内部的界面反应的演化、界面产物的组成和电子特性做了详细分析。包括常见氧化物正极及包覆材料与不同硫化电解质之间的化学和电化学反应以及电解质自身的电化学氧化分解。研究发现氧化物正极与硫化物电解质在外加化学势下的界面反应(电化学反应)驱动力远大于化学反应,主导着界面反应。氧化物正极与电解质的界面化学和电化学反应生成大量过渡金属硫化物分布在界面层为界面电化学反应发生提供电子导电网络导致界面的持续恶化。减少界面层中电子导电产物的摩尔百分比对有效降低界面层的电子电导,从而提升正极与电解质的界面兼容性至关重要。通过优化正极/电解质匹配和引入合适包覆材料可以有效的降低界面层中的电子导电产物的摩尔百分比。该工作以“The nature and suppression strategies of interfacial reactions in all-solid-state batteries”为题发表在国际期刊Energy&Environmental Science上。任福成是本文的第一作者。
【内容详情】
1.复合正极中的界面和界面反应
复合正极制备过程中需要将正极,电解质和导电炭混合,导致在未包覆处理的复合正极中存在诸多界面如图1所示。这些界面为副反应提供场所,而所有的界面反应可以分为两类:界面化学反应和界面电化学反应。一般认为固体电解质与导电炭/集流体化学稳定,而氧化物正极与硫化物电介质热力学不稳定易发生界面化学反应。界面电化学反应包括电解质在导电炭/集流体表面发生电化学氧化分解,以及正极/电解质界面在电池循环过程中的界面电化学反应。电解质氧化产物为电子绝缘体可以钝化其表面而有效阻止其持续氧化。正极/电解质界面的化学和电化学反应直接造成全固态电池容量衰减。
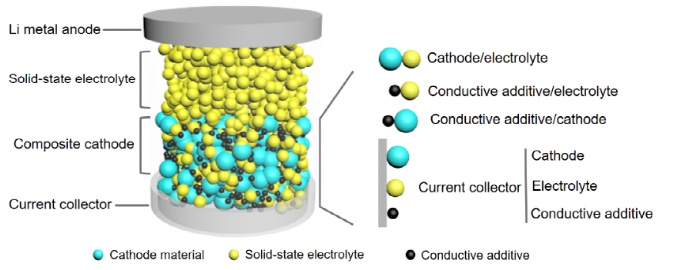
图1.未包覆处理复合正极中的界面示意图。
2.氧化物正极与硫化电解质化学和电化学兼容性
氧化物正极与电解质的化学反应性与正极材料脱锂状态相关,正极材料锂含量越低,界面反应性越强,例如L0.5CO/LPS界面反应能比LCO/LPS高153mev/atom。在相同嵌锂状态下,氧化物正极与电解质的电化学反应驱动力明显大于化学反应,且随电压升高(锂化学势降低)反应能明显增大,例如L0.5NMO/LPSCl电化学反应能比其化学反应能高998mev/atom,比LNMO/LPSCl电化学反应能高994mev/atom。常见氧化物正极中只有LiFePO4与硫化物电解质具有较好的化学兼容性(~242mev/atom),但在电化学条件下,其反应能也明显增大(~979mev/atom)。说明在电池循环过程中正极/电解质之间的界面电化学反应对电池的影响更大。

图2.氧化物正极与硫化物电解质化学和电化学反应能(图片和图片)。化学反应能:a)正极满嵌锂态,c)正极半嵌锂态。电化学反应:b),正极满嵌锂态,外加化学势图片,d)正极半嵌锂态,外加化学势图片。
3.不同电压下的复合正极中的界面恶化机制
在不同化学势下,复合正极中各界面的化学和电化学反应程度不同导致不同的界面失效机制,在低电压下正极/电解质界面的化学和电化学反应性明显强于电解质自身的氧化分解,导致界面阻抗增加。在高电压下,由于电压已经远高于电解质自身的稳定电化学窗口,在集流体/导电炭界面电解质发生严重的氧化分解,生成S,P2S7等不含锂和低锂含量的产物,破坏电解质结构,导致电解质自身的锂离子电导率降低,从而使得复合正极中的锂离子电导率下降。
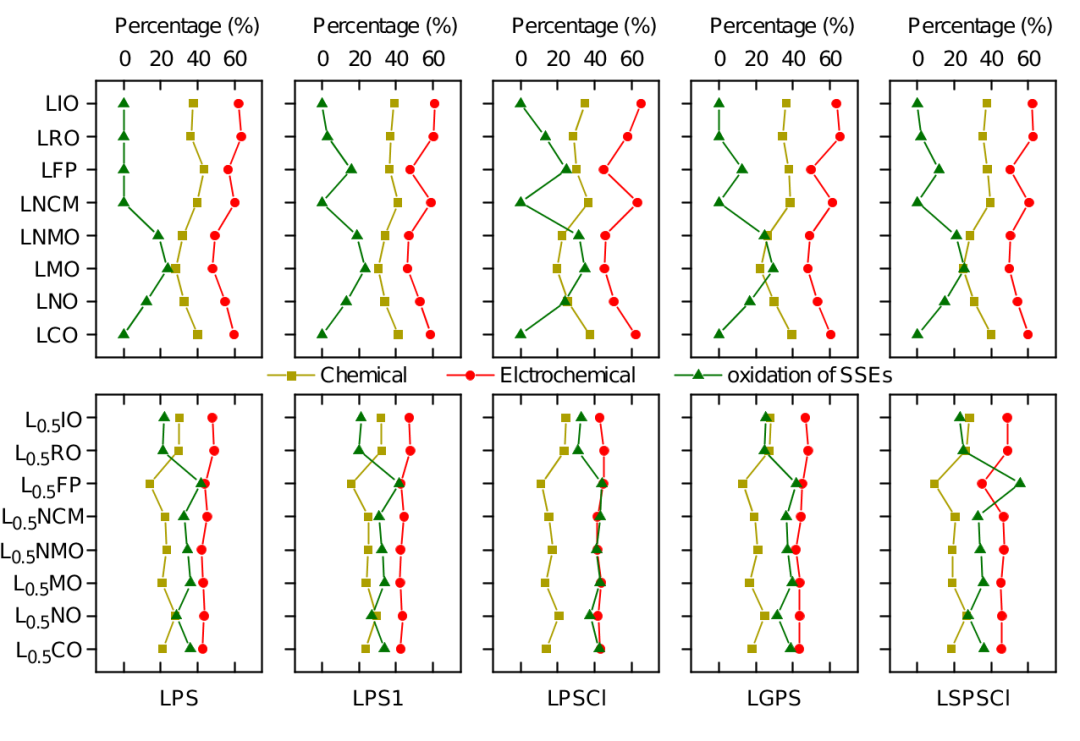
图3.不同嵌锂态下正极与电解质化学和电化学反应能及硫化物电解质自身电化学分解能占比(满嵌锂态-顶部,半嵌锂态-底部)。
4.界面层电子电导
以上研究表明复合正极中的界面电化学反应对全固态电池的循环性能,容量保持率以及阻抗有更显著的影响,但其持续发生的前提是界面层要有足够的电子电导。通过热力学相平衡分析发现在正极/电解质的化学和电化学相平衡中生成大量的带隙值为零的过渡金属硫化物,这些产物作为电子导体布在界面层形成电子导电网络导致界面电化学反应在循环中持续发生,恶化复合正极中的界面,从而导致界面阻抗的持续增加,和容量衰退。作者首次提出用界面层中带隙小于0.5eV的相在所有界面产物中所占的摩尔百分比(图片)描述界面层的电子电导,图4(a)。图片越大,界面层电子导电性越强,界面电化学反应越容易发生。降低界面层的电子电导可以有效抑制界面电化学反应发生,提升正极/电解质界面兼容性和全固态电池的循环性能。
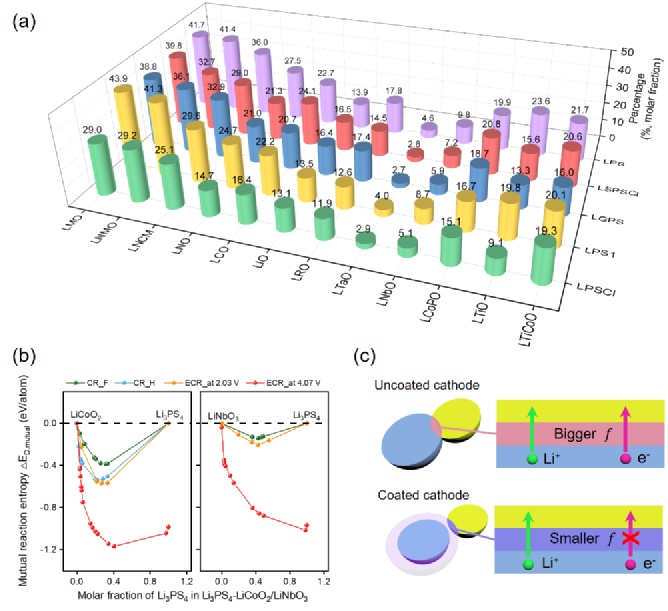
图4.(a)正极和电解质界面反应形成的界面相中,带隙小于0.5eV的相的摩尔百分比。(b)Li3PS4与LiCoO2/LiNbO3之间的化学/电化学反应能。(c)不同类型界面层示意图。
5.二元硫化物带隙
含锂氧化物材料与硫化电解质界面反应生成大量过渡金属硫化物(MxSy),这些过渡金属硫化物的电子导电对界面电化学稳定性具有决定性作用。全固态电池实现高容量保持率,长循环性能,包覆层有着十分重要的作用。包覆材料与硫化物电解质并非绝对稳定,在外加化学势条件下仍然具有很强的电化学反应性(图4b),所以在包覆材料的选择过程中需要避免电子导电产物的生成从而更好的钝化界面。大部分3d过渡金属对应的二元硫化物带隙值均<0.5eV不利于钝化界面的形成,而且是常见氧化物正极材料的关键组成元素。
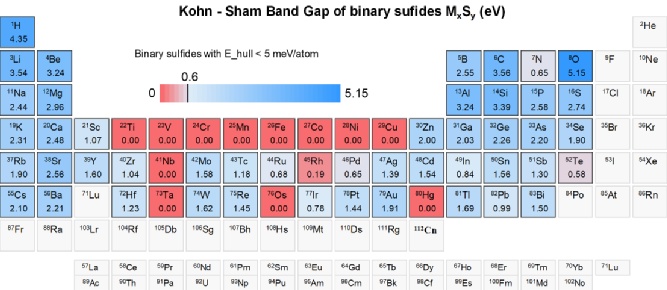
图5.元素周期表中所有元素对应二元硫化物的带隙。
6.包覆材料筛选
在包覆材料的筛选过程中需要考虑多重因素:材料的电子电导(Eg>0.5eV),相稳定性,与硫化物电解质反应不生成电子导电相、与电解质和正极化学稳定性,同时具备快离子导体的结构特征和低锂离子扩散能。从17082中含锂化合物中筛选出48中包覆材料,多种快离子导体(LiTaSiO4,Li3Sc(BO3)2,Li3InCl6,Li3ErBr6,LiAlCl4等)出现在筛选结果中,且与正极/电解质同时具有较好的化学稳定性,证实了筛选条件的合理性和有效性。
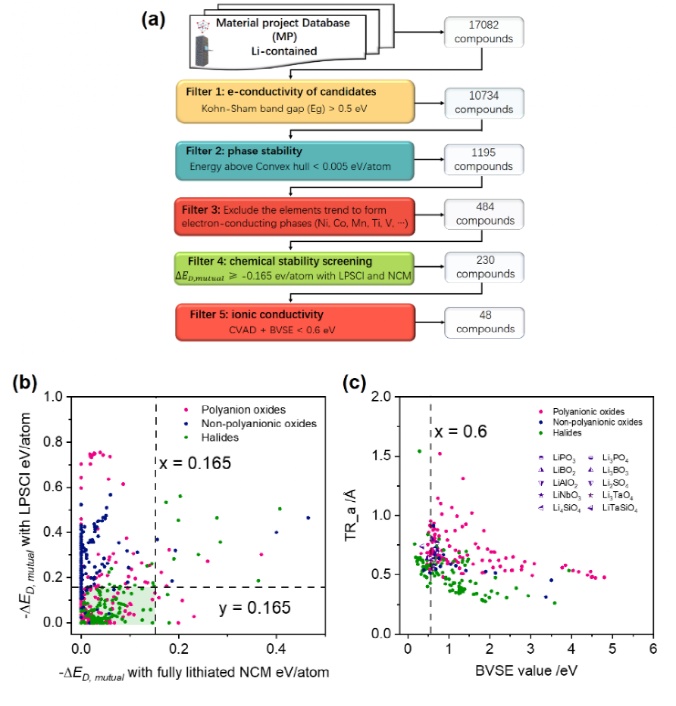
图6.(a)包覆材料筛选流程。(b)候选包覆材料与Li6PS5Cl(LPSCl)和LiNi1/3Co1/3Mn1/3O2(NCM)化学反应能。(c)通过化学反应能筛选的候选材料沿a方向的扩散瓶颈尺寸与扩散能垒(BVSE)。
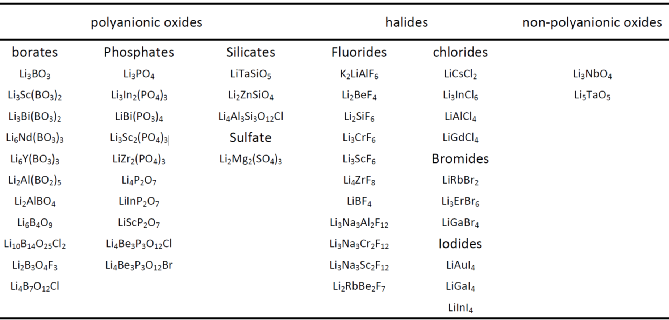
表1.包覆材料筛选结果
【结论】
本文系统地研究了基于硫化物固体电解质的复合正极中界面反应的演化过程,包括正极和电解质之间的化学和电化学反应,以及电解质自身的电化学分解,并对界面产物的组成和电子电导性做了详细分析。结果表明,正极与电解质之间的电化学反应驱动力大约是化学反应驱动力的两倍(满/半嵌锂态),主导着正极/电解质的界面反应。常用氧化物正极和电解质之间的界面反应生成大量零带隙的过渡金属硫化物(MxSy),作为电子导体分布在界面层形成电子导电网络。界面层的电子电导在诱发界面电化学反应中至关重要,也是长循环过程中正极和电解质界面兼容性的一个重要指标。作者首次提出利用界面产物中电子导电相的摩尔百分比(图片)作为界面的电化学稳定性描述子。低图片界面有利于抑制界面电化学反应在循环过程持续发生,形成薄的界面钝化层。相比于其它硫化物电解质,LPSCl与氧化物正极匹配所形成界面层的图片最小,因此表现出更好的界面稳定性和优异的循环稳定性。合理选择包覆材料可以进一步提升复合正极中的界面稳定性,作者提出了一种高通量筛选方案来筛选高性能包覆材料。综合考虑了材料的电子和离子电导率、相稳定性、形成的界面层的电子电导率以及与正极/电解质的化学稳定性,最终筛选出48种对正极和电解质均表现出良好的化学稳定性,并具有高锂离子电导率的包覆材料。本研究为正极和电解质的合理匹配提供了有价值的指导,并为包覆材料的选择提供了标准,以促进全固态电池高容量保持率和长循环性能的实现。
(中国粉体网编辑整理/文正)
注:图片非商业用途,存在侵权告知删除!

















